Zgodnie z modelem atomowym Nielsa Bohra protony i neutrony atomu znajdują się w jądrze, a elektrony wokół niego. Chociaż nie możemy dokładnie wiedzieć, gdzie znajduje się elektron, istnieją obszary, w których najprawdopodobniej można go znaleźć, orbitale atomowe. A jak możemy określić te orbitale? Bardzo proste, używając liczb kwantowych.
Jakie są liczby kwantowe?
Istnieją 4 liczby kwantowe. Trzy z nich dają nam informacje o tym, gdzie znajduje się elektron danego atomu, czyli dają nam informacje o orbicie. Z drugiej strony czwarta liczba kwantowa nie mówi nam, gdzie jest elektron, ale jak. Czy nadal nie jest to jasne? Idź po to!
- Główna liczba kwantowa (n). Jest to ostatni poziom energii do wypełnienia i wskazuje wielkość orbity, a tym samym odległość między jądrem a elektronem. Czemu? Bardzo łatwe. Im większy orbital, tym dalej elektron może znajdować się od jądra atomu.
- Azymutalna lub wtórna liczba kwantowa (l). Wskaż kształt orbitalu.
- Magnetyczna liczba kwantowa (m). Wskazuje orientację orbitalu.
- Zakręć liczbę kwantową (s). Powiedz, w którą stronę obraca się elektron.
Łatwe, prawda? Przejdźmy do ważnej rzeczy!
Jak wyprowadza się liczby kwantowe
Aby uzyskać liczby kwantowe, wystarczy wykonać 2 proste kroki:
- Napisz konfigurację elektronową.
- Pobierz liczby kwantowe z elektronu różniczkowego (ostatniego, który wypełnia orbitę).
Elektroniczna Konfiguracja
Zaczynamy od kroku 1, piszemy konfigurację elektronów. Jak? Są na to dwa sposoby, przejdźmy do tego!
Wykres Moellera
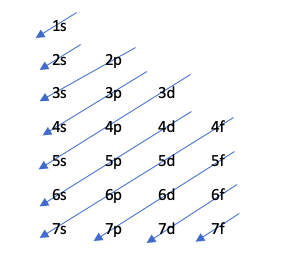
Ta technika wskazuje kolejność wypełniania orbitali za pomocą następującego rysunku:
Ten diagram rządzi się zasadą Aufbau, która broni tego, że orbitale wypełniają się w porządku rosnącym energią, to znaczy orbital, który ma najmniej energii, zapełni się wcześniej.
Aby dowiedzieć się, który orbital ma więcej energii, wykonywana jest operacja n + l. Jeśli ta operacja dla dwóch różnych atomów da w wyniku tę samą liczbę, to ten, którego liczba n jest wyższa, będzie miał więcej energii. Innymi słowy, w przypadku remisu, ta z najmniejszą liczbą n jest wypełniana jako pierwsza. Zobaczmy to na przykładzie:
4p: n + l -> 4 + 1 = 5
5s: n + l -> 5 + 0 = 5
Ponieważ istnieje remis w regule n + l, wypełnia ona 4p wcześniej, ponieważ jej liczba n jest mniejsza.
Model jądra
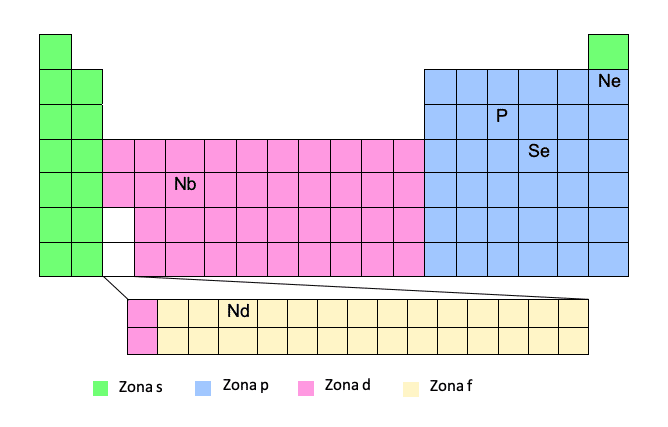
Aby uzyskać konfigurację elektroniczną zgodną z tym modelem, trzeba bardzo dobrze znać układ okresowy. Jeśli mamy liczbę atomową i pozycję pierwiastka w tabeli, to bułka z masłem!
Ta metoda jest uważana za metodę uproszczoną, ponieważ pozwala nie pisać pełnej konfiguracji elektronowej. W ten sposób możemy w nawiasie wpisać nazwę elementu gazu szlachetnego, a następnie ścieżkę od tego gazu do danego pierwiastka. Zobaczmy przykład:W ten sposób zapiszemy trajektorię uwzględniając numer okresu (wiersz układu okresowego) i „strefę”, a po zapisaniu konfiguracji elektronicznej wydobędziemy liczby kwantowe.
Luminofor (P) zostanie zapisany z poprzedniego gazu szlachetnego, czyli Neon:
P -> [Ne] 3s23p3
Oczywiście musisz być ostrożny z tą metodą, ponieważ strefy d i f są strefami specjalnymi. W trakcie podróży w strefie d nie będziemy umieszczać numeru okresu (wiersza), ale numer okresu minus jeden. To samo dzieje się z obszarem F, nie podamy numeru okresu, ale numer okresu minus dwa. Zrozumiesz to lepiej na kilku przykładach:
Nb -> [Kr] 5s14d4
Chociaż jest to w okresie 5, kiedy jesteśmy w strefie d, odejmujemy 1.
Nd -> [Xe] 6s24f14
Chociaż jest to w okresie 6, kiedy jesteśmy w strefie f, odejmujemy 2.
Wyjątki w konfiguracji elektronicznej
Konfiguracja elektronowa ma kilka szczególnych aspektów, które, jeśli nie są tego świadome, mogą prowadzić do dużych podajników głowic. Ale nie siej paniki! Powiemy Ci!
Strefa F
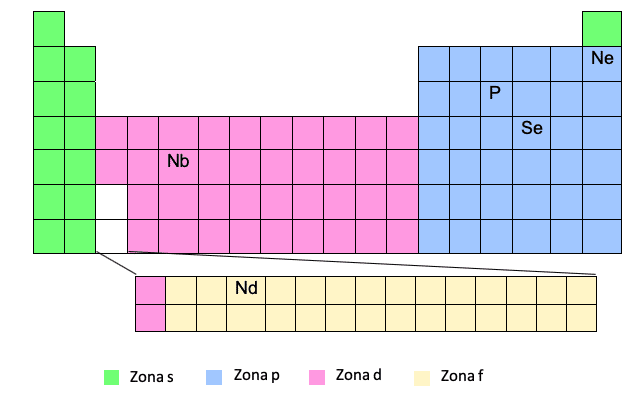
Strefa F pojawia się na dole układu okresowego, ale w rzeczywistości jest „wbudowana” w przerwę, którą widzimy na biało, to znaczy między pierwszym i drugim elementem ostatnich dwóch rzędów strefy D.
Widzisz to? Dlatego czasami, gdy musimy zapisać konfigurację elektroniczną elementu w strefie F, na przykład Nd, będziemy musieli umieścić elektron w strefie D odpowiedniego poziomu w odniesieniu do tego elementu w strefie D, który jest przed wejściem strefa F.
Ce -> [Xe] 6s25d14f1
Grupa 6 i Grupa 11
Metale przejściowe z grupy 6 i 11 mają odpowiednio 4 i 9 elektronów w swoich ostatnich powłokach. Dlatego, aby być bardziej stabilnym pierwiastkiem, orbital s ulega wzbudzeniu i traci elektron, który przechodzi do następnego orbitalu, d. W ten sposób orbital s pozostanie z elektronem; oraz d z 5, jeśli jest elementem grupy 6, lub z 10, jeśli jest elementem grupy 11.
Oto przykład:
Ag -> [Kr] 5s24d9
Najwyraźniej byłaby to konfiguracja elektronowa srebra (Ag). Jednak tracąc elektron z orbitalu s wygląda to tak:
Ag -> [Kr] 5s14d10
Istnieją jednak wyjątki od tej reguły, takie jak wolfram (grupa 6), który pozostaje z 2 elektronami na orbicie s i 4 na orbicie d.
Ale nie martw się, najbardziej typowe (Cr, Cu, Ag i Au) przestrzegają tej zasady.
Rozumiesz? Dobrze. To wszystko, co musisz wiedzieć o konfiguracji elektronów. Przejdźmy do liczb kwantowych!
Jak uzyskać liczby kwantowe
Aby uzyskać liczby kwantowe, musimy wiedzieć, ile elektronów mieści się w każdej powłoce orbitalnej, biorąc pod uwagę, że na orbitę mieszczą się 2 elektrony.
- Warstwa s. Ma tylko jeden orbital, więc może pomieścić 2 elektrony.
- Warstwa p. Ma 3 orbitale, więc jest miejsce na 6 elektronów.
- Warstwa d. Ma 5 orbitali, więc może zmieścić 10 elektronów.
- Warstwa f. Ma 7 orbitali, czyli zawiera 14 elektronów.
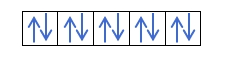
Teraz, gdy rozumiesz, że na każdym orbicie znajdują się 2 elektrony, powinieneś znać zasadę Hunda. Zasada ta mówi, że podczas wypełniania orbitali tego samego podpoziomu lub powłoki, na przykład powłoki p, elektrony wypełniają orbital w jednym kierunku (dodatni), a potem w drugim (ujemnym). Chcesz to zobaczyć na przykładzie?
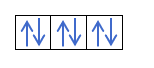
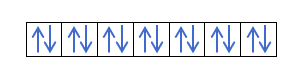
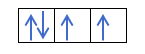
Jeśli mamy 2p4, czyli orbital 2p z 4 elektronami, nie wypełni się tak:
Wypełni się tak:
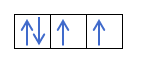
Czy to rozumiesz? Świetnie, zobaczmy, jak obliczyć liczby:
- Liczba kwantowa n. Liczba ta pokrywa się z numerem ostatniego poziomu konfiguracji elektronowej. Na przykład, jeśli konfiguracja elektronowa kończy się na 4s2, główna liczba kwantowa wyniesie 4.
- Liczba kwantowa l. Ta liczba zależy od ostatniej wypełnionej warstwy.
- Warstwa s -> l = 0
- Warstwa p -> l = 1
- Warstwa d -> l = 2
- Warstwa f -> l = 3
- Liczba kwantowa m. Liczba m może być dowolną wartością z zakresu od -l do + l, więc będzie zależeć od podpoziomu, w którym znajduje się elektron różniczkowy, to znaczy od tego, czy jest to s, p, d czy f. Obliczenie tej liczby jest nieco bardziej skomplikowane, zobaczmy to na kilku rysunkach:
- Warstwa s -> Jak widzieliśmy, l ma wartość 0, więc m może być warte tylko 0.
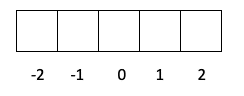
- Warstwa p -> l ma wartość 1, więc m może wynosić -1, 0 lub 1.
- Warstwa d -> l wynosi 2, więc m może wynosić -2, -1, 0, 1 i 2.
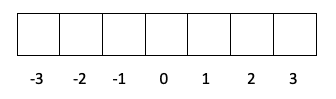
- Warstwa f -> l ma wartość 3, więc m może wynosić -3, -2, -1, 0, 1, 2 i 3.
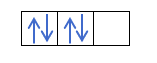
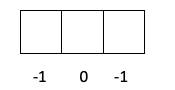
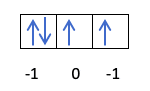
Wiesz już, w jaki sposób orbitale są wypełnione, więc liczba kwantowa m będzie miała wartość dziury, w której znajduje się ostatni narysowany elektron. Czy pamiętasz ten przykład sprzed?:
W tym przypadku m będzie wynosić -1, ponieważ w powłoce p (3 orbitale), jeśli są 4 elektrony, ostatni do wypełnienia byłby ujemny względem pierwszego orbitala.
- Liczby kwantowe. Liczba kwantowa s może być warta tylko ½ i -½. Jeśli ostatni wyciągnięty elektron jest dodatni, to znaczy strzałka jest skierowana w górę, s będzie wynosić ½. Z drugiej strony, jeśli ostatni elektron, który wypełnił orbitę, jest ujemny, to znaczy ze strzałką skierowaną w dół, s będzie wynosić -½.
Ćwiczenia i przykłady
Tak, już wiemy, że to wszystko to dużo informacji, ale zrozumiesz to lepiej na kilku przykładach. No to ruszamy!
Przykład 1
Selen (Se) -> Liczba atomowa: 34
- Piszemy konfigurację elektronową. Konfigurację elektronów piszemy zgodnie z diagramem Moellera, biorąc pod uwagę, że orbitale s, p, d i f mają odpowiednio 2, 6, 10 i 14 elektronów. Konfigurację zapisujemy dodając liczbę elektronów, która jest zapisywana jako wykładnik.
1s22s22p63s23p64s23d104p4
Ponieważ orbital 4p się nie wypełnia, ponieważ elektrony sumują się do 36, nie umieszczamy 4p6ale 4p4.
- Wyjmujemy liczby kwantowe. Aby to zrobić, przyglądamy się elektronowi walencyjnemu lub różniczkowemu, czyli ostatniemu elektronowi, który wypełnił orbitę. W tym przypadku przyjrzymy się 4p4.
- Główna liczba kwantowa. Ostatni poziom energii do wypełnienia wynosił 4.
n = 4
- Wtórna liczba kwantowa. Ostatnim podpoziomem energii do wypełnienia był orbital p.
l = 1
- Magnetyczna liczba kwantowa. Jeśli rysujemy elektrony, ostatnim do wypełnienia będzie pierwszy orbital powłoki p.
m = -1
- Spinowa liczba kwantowa. Ostatni elektron zajmujący orbitę p ma strzałkę w dół.
s = -½
Przykład 2
Złoto (Au) -> [Xe] 6s14f145d10
- Główna liczba kwantowa -> n = 5
- Drugorzędna liczba kwantowa -> l = 2
- Magnetyczna liczba kwantowa -> m = 2
- Zakręć liczbę kwantową -> s = -½
I to wszystko! Teraz twoja kolej, czy mógłbyś zrobić konfigurację elektronową i uzyskać liczby kwantowe następujących pierwiastków?:
Cr(24), Rb(37), Br(35), Lu(71), Au(79)