ตามแบบจำลองอะตอมของ Niels Bohr โปรตอนและนิวตรอนของอะตอมอยู่ในนิวเคลียส ในขณะที่อิเล็กตรอนอยู่รอบๆ แม้ว่าเราจะไม่สามารถทราบได้ว่าอิเล็กตรอนอยู่ที่ไหนกันแน่ แต่ก็มีพื้นที่ที่น่าจะพบมากที่สุด นั่นคือ ออร์บิทัลของอะตอม และเราจะกำหนดออร์บิทัลเหล่านั้นได้อย่างไร? ง่ายมาก โดยใช้ตัวเลขควอนตัม
ตัวเลขควอนตัมคืออะไร?
มี 4 ตัวเลขควอนตัม สามคนให้ข้อมูลกับเราว่าอิเล็กตรอนของอะตอมหนึ่งอยู่ที่ไหน นั่นคือ ให้ข้อมูลเกี่ยวกับวงโคจรแก่เรา ในทางกลับกัน หมายเลขควอนตัมที่สี่ไม่ได้บอกเราว่าอิเล็กตรอนอยู่ที่ไหน แต่เป็นอย่างไร คุณยังไม่ชัดเจนเกี่ยวกับเรื่องนี้หรือไม่? ไปหามัน!
- หมายเลขควอนตัมหลัก (NS). เป็นระดับพลังงานสุดท้ายที่จะเติมและระบุขนาดของวงโคจรและระยะห่างระหว่างนิวเคลียสกับอิเล็กตรอน ทำไม? ง่ายมาก. ยิ่งวงโคจรมีขนาดใหญ่เท่าใด อิเล็กตรอนก็จะยิ่งอยู่ห่างจากนิวเคลียสของอะตอมมากขึ้นเท่านั้น
- Azimuthal หรือเลขควอนตัมทุติยภูมิ (ล). ระบุรูปร่างของวงโคจร
- เลขควอนตัมแม่เหล็ก (NS). ระบุทิศทางของวงโคจร
- หมุนหมายเลขควอนตัม (NS). บอกว่าอิเล็กตรอนหมุนไปทางไหน
ง่ายใช่มั้ย? ลุยกันต่อกับของสำคัญ!
ตัวเลขควอนตัมได้มาอย่างไร
เพื่อให้ได้ตัวเลขควอนตัม คุณเพียงแค่ทำตาม 2 ขั้นตอนง่ายๆ:
- เขียนการกำหนดค่าอิเล็กตรอน
- หาเลขควอนตัมจากอิเล็คตรอนดิฟเฟอเรนเชียล
การกำหนดค่าอิเล็กทรอนิกส์
เราเริ่มต้นด้วยขั้นตอนที่ 1 เขียนการกำหนดค่าอิเล็กตรอน ยังไง? มีสองวิธีในการทำ มาเริ่มกันเลย!
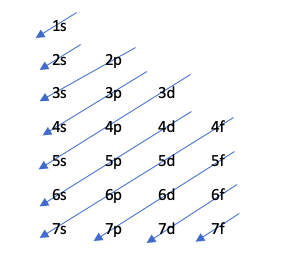
แผนภาพ Moeller
เทคนิคนี้ระบุลำดับของการเติม orbitals ผ่านภาพวาดต่อไปนี้:
แผนภาพนี้ควบคุมโดยหลักการของ Aufbau ซึ่งระบุว่าออร์บิทัลนั้นเต็มไปด้วยลำดับของพลังงานที่เพิ่มขึ้น กล่าวคือ ออร์บิทัลที่มีพลังงานน้อยที่สุดจะเติมก่อนหน้านี้
เพื่อหาว่าวงโคจรใดมีพลังงานมากกว่า การดำเนินการ n + l จะดำเนินการ หากการดำเนินการนี้สำหรับอะตอมที่ต่างกันสองอะตอมส่งผลให้เกิดเลขเดียวกัน เลข n ที่สูงกว่าจะมีพลังงานมากกว่า กล่าวอีกนัยหนึ่ง ในกรณีที่เสมอกัน ให้เติมตัวที่มีตัวเลข n ต่ำที่สุดก่อน ลองดูด้วยตัวอย่าง:
4p: n + l -> 4 + 1 = 5
5s: n + l -> 5 + 0 = 5
เนื่องจากมีการเสมอกันในกฎ n + l มันจึงเติม 4p ก่อนหน้านั้นเพราะเลข n ต่ำกว่า
โมเดลเคอร์เนล
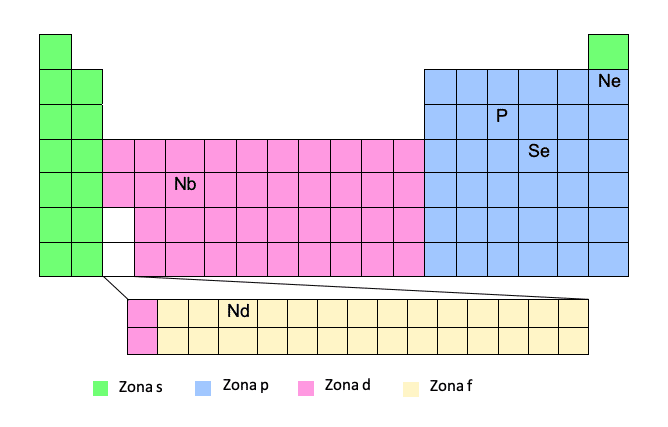
เพื่อให้ได้การกำหนดค่าทางอิเล็กทรอนิกส์ตามแบบจำลองนี้ คุณต้องรู้จักตารางธาตุเป็นอย่างดี ถ้าเรามีเลขอะตอมและตำแหน่งของธาตุในตาราง นั่นก็เป็นเรื่องกล้วยๆ!
วิธีนี้ถือเป็นวิธีการแบบง่าย เนื่องจากช่วยให้ไม่ต้องเขียนการกำหนดค่าอิเล็กตรอนแบบสมบูรณ์ ด้วยวิธีนี้ เราสามารถเขียนชื่อของธาตุก๊าซมีตระกูลด้านบนในวงเล็บ และจากนั้นเส้นทางจากก๊าซมีตระกูลนั้นไปยังธาตุที่เป็นปัญหา มาดูตัวอย่างกัน:ดังนั้น เราจะเขียนวิถีโดยคำนึงถึงจำนวนของคาบ (แถวของตารางธาตุ) และ "พื้นที่" และเมื่อเขียนการกำหนดค่าอิเล็กตรอนแล้ว เราจะแยกตัวเลขควอนตัมออกมา
สารเรืองแสง (P) จะถูกเขียนจากก๊าซมีตระกูลก่อนหน้านั่นคือ Neon:
P -> [Ne] 3s23p3
แน่นอน คุณต้องระวังด้วยวิธีนี้ เนื่องจากโซน d และ f เป็นโซนพิเศษ ขณะที่เราเดินทาง ในโซน d เราจะไม่ใส่จำนวนงวด (แถว) แต่จำนวนงวดลบหนึ่ง เช่นเดียวกันกับพื้นที่ F เราจะไม่ใส่จำนวนงวด แต่จำนวนงวดลบสอง คุณจะเข้าใจดีขึ้นด้วยตัวอย่างสองสามตัวอย่าง:
Nb -> [Kr] 5s14d4
แม้ว่าจะอยู่ในคาบ 5 แต่เมื่อเราอยู่ในโซน d เราลบ 1
Nd -> [Xe] 6s24f14
แม้ว่าจะอยู่ในคาบ 6 แต่เมื่อเราอยู่ในโซน f เราลบ 2
ข้อยกเว้นในการกำหนดค่าอิเล็กทรอนิกส์
การจัดโครงแบบอิเล็กตรอนมีลักษณะพิเศษสองสามประการ ซึ่งหากคุณไม่ทราบลักษณะเหล่านี้ อาจทำให้คุณมีหัวป้อนขนาดใหญ่ แต่อย่ากระจายความตื่นตระหนก! เราจะบอกคุณ!
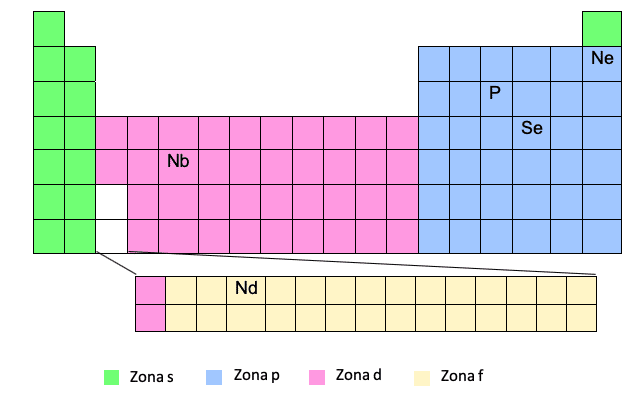
โซน F
โซน F ปรากฏขึ้นที่ด้านล่างของตารางธาตุ แต่จริงๆ แล้ว "ฝัง" ในช่องว่างที่เราเห็นเป็นสีขาว นั่นคือระหว่างองค์ประกอบที่หนึ่งและที่สองของสองแถวสุดท้ายของโซน D
คุณเห็นมันไหม ด้วยเหตุนี้ บางครั้ง เมื่อเราต้องเขียนโครงร่างอิเล็กทรอนิกส์ขององค์ประกอบในโซน F เช่น Nd เราจะต้องใส่อิเล็กตรอนในโซน D ของระดับที่สอดคล้องกันในการอ้างอิงถึงองค์ประกอบนั้นในโซน D นั่นคือ ก่อนเข้าโซน F.
Ce -> [Xe] 6s25d14f1
กลุ่ม 6 และกลุ่ม 11
โลหะทรานซิชันกลุ่มที่ 6 และกลุ่มที่ 11 มีอิเล็กตรอน 4 และ 9 ในเปลือกสุดท้ายตามลำดับ ดังนั้น เพื่อเป็นองค์ประกอบที่มีเสถียรภาพมากขึ้น s ออร์บิทัลจะตื่นเต้นและสูญเสียอิเล็กตรอนซึ่งส่งผ่านไปยังออร์บิทัลถัดไป d ด้วยวิธีนี้ s ออร์บิทัลจะเหลืออิเล็กตรอน และ d ด้วย 5 ถ้าเป็นองค์ประกอบของกลุ่ม 6 หรือ 10 ถ้าเป็นองค์ประกอบของกลุ่ม 11
นี่คือตัวอย่าง:
Ag -> [Kr] 5s24d9
เห็นได้ชัดว่านี่คือการกำหนดค่าอิเล็กตรอนของเงิน (Ag) อย่างไรก็ตามการสูญเสียอิเล็กตรอนจากวงโคจรจะมีลักษณะดังนี้:
Ag -> [Kr] 5s14d10
อย่างไรก็ตาม มีข้อยกเว้นสำหรับกฎนี้ เช่น ทังสเตน (กลุ่ม 6) ซึ่งเหลืออิเล็กตรอน 2 ตัวในวงโคจร s และ 4 ตัวในวงโคจร d
แต่ไม่ต้องกังวล คนทั่วไปส่วนใหญ่ (Cr, Cu, Ag และ Au) ปฏิบัติตามกฎนี้
คุณเข้าใจไหม? ดี. นั่นคือทั้งหมดที่คุณต้องรู้เกี่ยวกับการกำหนดค่าอิเล็กตรอน ไปหาตัวเลขควอนตัมกันเถอะ!
วิธีรับตัวเลขควอนตัม
เพื่อให้ได้ตัวเลขควอนตัม เราต้องรู้ว่ามีอิเล็กตรอนกี่ตัวที่พอดีกับเปลือกออร์บิทัลแต่ละอัน โดยพิจารณาว่าอิเล็กตรอน 2 ตัวพอดีในออร์บิทัล
- ชั้น s. มีออร์บิทัลเพียง 2 ออร์บิทัล จึงสามารถบรรจุอิเล็กตรอนได้ XNUMX ตัว
- เลเยอร์ p. มี 3 ออร์บิทัล จึงมีที่ว่างสำหรับอิเล็กตรอน 6 ตัว
- เลเยอร์d. มีออร์บิทัล 5 ออร์บิทัล จุอิเล็กตรอนได้ 10 อิเล็กตรอน
- เลเยอร์f. มี 7 ออร์บิทัล นั่นคือ จุอิเล็กตรอนได้ 14 อิเล็กตรอน
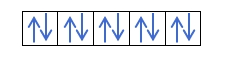
เมื่อคุณเข้าใจแล้วว่าอิเล็กตรอน 2 ตัวพอดีในแต่ละออร์บิทัล คุณต้องรู้กฎของฮันด์ กฎข้อนี้กล่าวว่าเมื่อเติมออร์บิทัลของระดับย่อยหรือเชลล์เดียวกัน ตัวอย่างเช่น p เชลล์ อิเล็กตรอนจะเติมออร์บิทัลในทิศทางเดียว (บวก) จากนั้นในอีกทางหนึ่ง (เชิงลบ) คุณต้องการดูตัวอย่างหรือไม่?
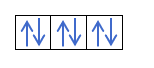
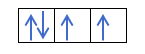
ถ้าเรามี 2p4นั่นคือวงโคจร 2p ที่มี 4 อิเล็กตรอนจะไม่เติมดังนี้:
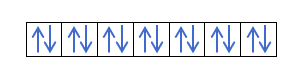
มันจะเติมดังนี้:
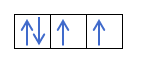
คุณได้รับมัน? เยี่ยมมาก เรามาดูวิธีการคำนวณตัวเลขกัน:
- หมายเลขควอนตัม n. ตัวเลขนี้ตรงกับจำนวนระดับสุดท้ายของการกำหนดค่าอิเล็กตรอน ตัวอย่างเช่น หากการกำหนดค่าอิเล็กตรอนสิ้นสุดใน 4s2เลขควอนตัมหลักจะเป็น 4
- หมายเลขควอนตัม l. ตัวเลขนี้ขึ้นอยู่กับเลเยอร์สุดท้ายที่เติม
- เลเยอร์ s -> l = 0
- เลเยอร์ p -> l = 1
- เลเยอร์ d -> l = 2
- เลเยอร์ f -> l = 3
- ควอนตัมจำนวน ม. ตัวเลข m สามารถเป็นค่าใดก็ได้ระหว่าง -l ถึง + l ดังนั้นมันจะขึ้นอยู่กับระดับย่อยที่อิเลคตรอนส่วนต่างคือ s, p, d หรือ f วิธีคำนวณตัวเลขนี้ซับซ้อนกว่าเล็กน้อยลองดูด้วยภาพวาดสองสามแบบ:
- เลเยอร์ s -> ดังที่เราได้เห็นแล้วว่า l มีค่าเป็น 0 ดังนั้น m จึงมีค่าเท่ากับ 0 เท่านั้น
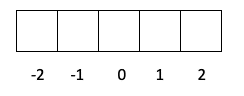
- Layer p -> l มีค่าเท่ากับ 1 ดังนั้น m สามารถเป็น -1, 0 หรือ 1
- เลเยอร์ d -> l คือ 2 ดังนั้น m อาจเป็น -2, -1, 0, 1 และ 2
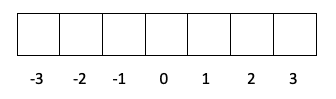
- เลเยอร์ f -> l มีค่า 3 ดังนั้น m สามารถเป็น -3, -2, -1, 0, 1, 2 และ 3
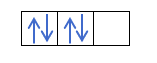
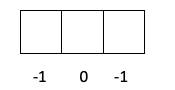
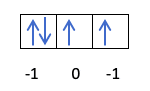
คุณรู้อยู่แล้วว่าออร์บิทัลถูกเติมอย่างไร ดังนั้นเลขควอนตัม m จะมีค่าเท่ากับรูที่อิเล็กตรอนถูกดึงตัวสุดท้ายออกมา คุณจำตัวอย่างนี้เมื่อก่อนได้ไหม :
ในกรณีนี้ m จะเป็น -1 เนื่องจากในเปลือก p (3 ออร์บิทัล) หากมีอิเล็กตรอน 4 ตัว อิเล็กตรอนตัวสุดท้ายที่เติมจะเป็นค่าลบของออร์บิทัลแรก
- จำนวนควอนตัม s. ตัวเลขควอนตัม s มีค่าเท่ากับ ½ และ -½ เท่านั้น ถ้าอิเล็กตรอนตัวสุดท้ายออกมาเป็นค่าบวก นั่นคือ ลูกศรขึ้น s จะเป็น ½ ในทางกลับกัน ถ้าอิเล็กตรอนตัวสุดท้ายที่เต็มวงโคจรเป็นลบ นั่นคือ เมื่อลูกศรชี้ลง s จะเป็น -½
แบบฝึกหัดและตัวอย่าง
ใช่ เรารู้แล้วว่าทั้งหมดนี้เป็นข้อมูลจำนวนมาก แต่คุณจะเข้าใจได้ดีขึ้นด้วยตัวอย่างบางส่วน ไปเลย!
ตัวอย่าง 1
ซีลีเนียม (Se) -> เลขอะตอม: 34
- เราเขียนการกำหนดค่าอิเล็กตรอน เรากำลังเขียนการกำหนดค่าอิเล็กตรอนตามแผนภาพ Moeller โดยคำนึงถึงว่าออร์บิทัล s, p, d และ f มี 2, 6, 10 และ 14 อิเล็กตรอนตามลำดับ เรากำลังเขียนการกำหนดค่าโดยการเพิ่มจำนวนอิเล็กตรอนซึ่งเขียนเป็นเลขชี้กำลัง
1s22s22p63s23p64s23d104p4
เนื่องจากออร์บิทัล 4p ไม่เติม เนื่องจากอิเล็กตรอนจะรวมกันได้ 36 เราจึงไม่ใส่ 4p6แต่ 4p4.
- เราเอาเลขควอนตัมออกมา ในการทำเช่นนี้ เราจะดูที่เวเลนซ์หรือดิฟเฟอเรนเชียลอิเล็กตรอน นั่นคือ อิเล็กตรอนตัวสุดท้ายที่เต็มออร์บิทัล ในกรณีนี้เราจะดูที่ 4p4.
- หมายเลขควอนตัมหลัก ระดับพลังงานสุดท้ายที่จะเติมคือ 4
n = 4
- หมายเลขควอนตัมรอง ระดับย่อยของพลังงานสุดท้ายที่จะเติมคือ p ออร์บิทัล
ล. = 1
- หมายเลขควอนตัมแม่เหล็ก หากเราวาดอิเล็กตรอน ตัวสุดท้ายที่เติมจะเป็นวงโคจรแรกของเปลือก p
ม. = -1
- หมุนหมายเลขควอนตัม อิเล็กตรอนตัวสุดท้ายที่ครอบครอง p orbital มีลูกศรลง
s = -½
ตัวอย่าง 2
ทอง (Au) -> [Xe] 6s14f145d10
- หมายเลขควอนตัมหลัก -> n = 5
- หมายเลขควอนตัมรอง -> ล. = 2
- เลขควอนตัมแม่เหล็ก -> ม. = 2
- หมุนหมายเลขควอนตัม -> s = -½
และนั่นคือทั้งหมด! ตอนนี้ถึงตาคุณแล้ว คุณช่วยจัดโครงอิเล็กตรอนและรับเลขควอนตัมขององค์ประกอบต่อไปนี้ได้ไหม:
Cr(24), Rb(37), Br(35), Lu(71), Au(79)