Enligt Niels Bohrs atommodell finns protoner och neutroner i en atom i kärnan, medan elektronerna är runt den. Även om vi inte kan veta var en elektron är exakt, finns det områden där den mest sannolikt finns, atomorbitalerna. Och hur kan vi bestämma dessa orbitaler? Mycket enkelt, med hjälp av kvantnummer.
Vad är kvantnumren?
Det finns 4 kvantnummer. Tre av dem ger oss information om var en elektron i en viss atom finns, det vill säga de ger oss information om orbitalet. Å andra sidan berättar det fjärde kvantnumret inte var elektronen är, utan hur. Är du fortfarande inte särskilt tydlig med detta? Gör det!
- Huvudkvantnummer (n). Det är den sista energinivån som fylls och anger storleken på orbitalet och därför avståndet mellan kärnan och elektronen. Varför? Väldigt lätt. Ju större orbital, desto längre kan elektronen vara från atomkärnan.
- Azimutalt eller sekundärt kvantnummer (l). Ange formen på banan.
- Magnetiskt kvantnummer (m). Anger orbitalets orientering.
- Snurra kvantnummer (s). Berätta på vilket sätt elektronen roterar.
Lätt eller hur? Låt oss gå med det viktiga!
Hur härleds kvantnummer
För att få kvantnumren behöver du bara följa 2 enkla steg:
- Skriv elektronkonfigurationen.
- Hämta kvantnumren från differentialelektronen (den sista som fyller orbitalet).
Elektronisk konfiguration
Vi börjar med steg 1, skriver elektronkonfigurationen. Hur? Det finns två metoder för att göra det, låt oss komma till det!
Moeller diagram
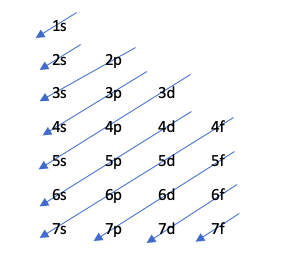
Denna teknik anger ordningen för fyllning av orbitalerna genom följande ritning:
Detta diagram styrs av Aufbau -principen, som försvarar att orbitalerna fyller i ökande energiordning, det vill säga den orbital som har minst energi kommer att fyllas tidigare.
För att ta reda på vilken orbital som har mer energi utförs operationen n + l. Om denna operation för två olika atomer resulterar i samma tal, kommer den vars nummer n är högre att ha mer energi. Med andra ord fylls den med det lägsta talet n vid ett oavgjort resultat. Låt oss se det med ett exempel:
4p: n + l -> 4 + 1 = 5
5s: n + l -> 5 + 0 = 5
Eftersom det är lika med n + l -regeln fyller den 4p tidigare eftersom dess antal n är lägre.
Kärnmodell
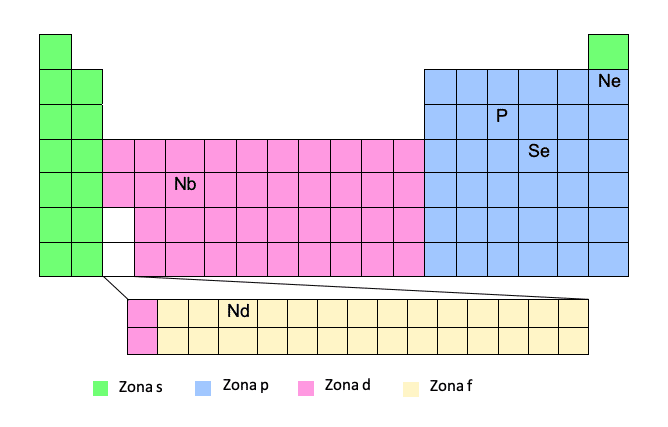
För att få den elektroniska konfigurationen efter denna modell måste du känna till det periodiska systemet mycket väl. Om vi har atomnumret och elementets position i tabellen är det en kaka!
Denna metod anses vara en förenklad metod eftersom den tillåter att du inte behöver skriva hela elektronkonfigurationen. På detta sätt kan vi skriva namnet på ädelgaselementet ovan inom parentes, och sedan vägen från den ädelgasen till elementet i fråga. Låt oss se ett exempel:Således kommer vi att skriva banan med hänsyn till periodens antal (rad i det periodiska systemet) och "området" och, när den elektroniska konfigurationen är skriven, kommer vi att extrahera kvantnumren.
Fosforet (P) kommer att skrivas från den tidigare ädelgasen, det vill säga neon:
P -> [Ne] 3s23p3
Naturligtvis måste du vara försiktig med denna metod, eftersom zonerna d och f är speciella zoner. När vi gör turen kommer vi i zon d inte att lägga till periodens (rad), utan periodens nummer minus en. Detsamma händer med zon F, vi kommer inte att sätta periodens nummer, utan periodens antal minus två. Du kommer att förstå det bättre med ett par exempel:
Nb -> [Kr] 5s14d4
Även om det är i period 5, när vi är i zon d, subtraherar vi 1.
Nd -> [Xe] 6s24f14
Även om det är i period 6, när vi är i zon f, subtraherar vi 2.
Undantag i den elektroniska konfigurationen
Elektronkonfigurationen har ett par speciella aspekter som, om du inte är medveten om dem, kan ge dig stora huvudmatare. Men sprid inte panik! Vi berättar!
Zon F
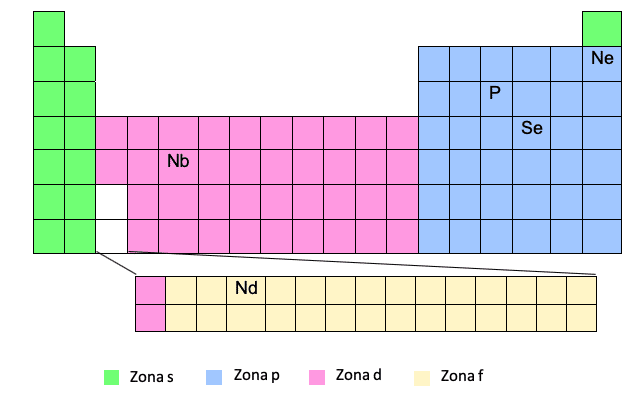
Zon F visas längst ner i det periodiska systemet, men är faktiskt "inbäddad" i gapet som vi ser i vitt, det vill säga mellan de första och andra elementen i de två sista raderna i zon D.
Du ser det? Av denna anledning, ibland, när vi måste skriva den elektroniska konfigurationen av ett element i zon F, till exempel Nd, måste vi sätta en elektron i zon D på motsvarande nivå med hänvisning till det elementet i zon D som är innan du går in i zon F.
Ce -> [Xe] 6s25d14f1
Grupp 6 och grupp 11
Grupp 6 och grupp 11 övergångsmetaller har 4 respektive 9 elektroner i sina sista skal, respektive. För att vara ett mer stabilt element blir s orbital därför upphetsad och förlorar en elektron, som passerar till nästa orbital, d. På detta sätt kommer s orbital att vara kvar med en elektron; och d med 5, om det är ett element i grupp 6, eller med 10, om det är ett element i grupp 11.
Här är ett exempel:
Ag -> [Kr] 5s24d9
Tydligen skulle detta vara elektronkonfigurationen av silver (Ag). Men när man tappar en elektron från s orbital ser den ut så här:
Ag -> [Kr] 5s14d10
Det finns dock undantag från denna regel, till exempel Tungsten (grupp 6), som är kvar med 2 elektroner i s orbital och 4 i d orbital.
Men oroa dig inte! De mest typiska (Cr, Cu, Ag och Au) följer denna regel.
Förstår du? Väl. Det är allt du behöver veta om elektronkonfiguration. Låt oss gå för kvantnummer!
Hur får man kvantnummer
För att få kvantnumren måste vi veta hur många elektroner som passar i varje orbitalskal, med tanke på att 2 elektroner passar in i en orbital.
- Skikten. Den har bara en orbital, så den kan passa 2 elektroner.
- Lager s. Den har 3 orbitaler, så det finns plats för 6 elektroner.
- Skikt d. Den har 5 orbitaler, så den rymmer 10 elektroner.
- Skikt f. Den har 7 orbitaler, det vill säga den rymmer 14 elektroner.
Nu när du förstår att det finns 2 elektroner i varje omlopp bör du känna till Hunds regel. Denna regel säger att när man fyller orbitaler av samma undernivå eller skal, till exempel p -skalet, fyller elektronerna orbitalet i en riktning (positivt) och sedan i den andra (negativa). Vill du se det med ett exempel?
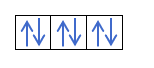
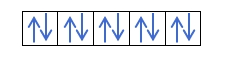
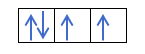
Om vi har 2p4, det vill säga 2p -orbitalet med 4 elektroner, fylls inte så här:
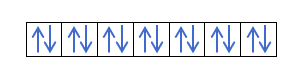
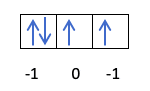
Det kommer att fyllas så här:
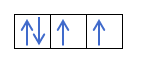
Fattar du det? Bra, låt oss se hur man beräknar siffrorna:
- Kvantnummer n. Detta nummer sammanfaller med numret på den sista nivån i elektronkonfigurationen. Till exempel om elektronkonfigurationen slutar på 4s2kommer huvudkvantumtalet att vara 4.
- Kvantnummer l. Detta nummer beror på det sista lagret som har fyllts.
- Skikt s -> l = 0
- Skikt p -> l = 1
- Skikt d -> l = 2
- Skikt f -> l = 3
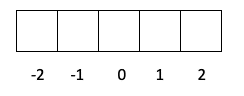
- Kvantnummer m. Talet m kan vara vilket värde som helst mellan -l till + l, så det beror på undernivån där differentialelektronen är, det vill säga om det är s, p, d eller f. Hur man beräknar detta nummer är lite mer komplicerat, låt oss se det med ett par ritningar:
- Skikt s -> Som vi har sett är l värt 0, så m kan bara vara värt 0.
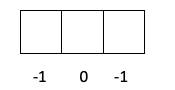
- Skikt p -> l är värt 1, så m kan vara -1, 0 eller 1.
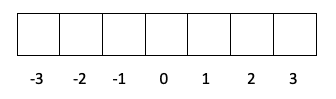
- Skikt d -> l är 2, så m kan vara -2, -1, 0, 1 och 2.
- Skikt f -> l är värt 3, så m kan vara -3, -2, -1, 0, 1, 2 och 3.
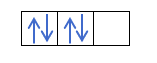
Du vet redan hur orbitalerna fylls, så kvantnumret m kommer att ha värdet av hålet där den senast dragna elektronen är. Kommer du ihåg detta exempel från tidigare?:
I detta fall kommer m att vara -1, eftersom i p -skalet (3 orbitaler), om det finns 4 elektroner, skulle den sista som ska fyllas vara negativet för den första orbitalen.
- Kvantnummer s. Kvantnumret s kan bara vara värt ½ och -½. Om den sista elektronen som dras är positiv, det vill säga att pilen är uppåt, blir s ½. Å andra sidan, om den sista elektronen för att fylla orbitalet är negativ, det vill säga med pilen pekande nedåt, blir s -½.
Övningar och exempel
Ja, vi vet redan att allt detta är mycket information, men du kommer att förstå det bättre med några exempel. Nu kör vi!
1 exempel
Selen (Se) -> Atomnummer: 34
- Vi skriver elektronkonfigurationen. Vi skriver elektronkonfigurationen enligt Moeller -diagrammet, med hänsyn till att orbitalerna s, p, d och f har 2, 6, 10 respektive 14 elektroner. Vi skriver konfigurationen genom att lägga till antalet elektroner, som skrivs som en exponent.
1s22s22p63s23p64s23d104p4
Eftersom 4p -orbitalet inte fylls upp, eftersom elektronerna skulle lägga till 36, lägger vi inte 4p6men 4p4.
- Vi tar ut kvantnumren. För att göra detta tittar vi på valens- eller differentialelektronen, det vill säga den sista elektronen som har fyllt orbitalet. I det här fallet kommer vi att titta på 4p4.
- Huvudkvantnummer. Den sista energinivån att fylla var 4.
n = 4
- Sekundärt kvantnummer. Den sista energinivån att fylla var p -orbitalet.
l = 1
- Magnetiskt kvantnummer. Om vi ritar elektronerna är den sista som ska fyllas den första orbitalen i p -skalet.
m = -1
- Snurra kvantnummer. Den sista elektronen som upptar p -orbitalet har nedåtpilen.
s = -½
2 exempel
Guld (Au) -> [Xe] 6s14f145d10
- Huvudkvantnummer -> n = 5
- Sekundärt kvantnummer -> l = 2
- Magnetiskt kvantnummer -> m = 2
- Snurra kvantnummer -> s = -½
Och det är allt! Nu är det din tur, kan du göra elektronkonfigurationen och få kvantnumren för följande element?:
Cr(24), Rb(37), Br(35), Lu(71), Au(79)